[vc_row][vc_column width=»1/4″][/vc_column][vc_column width=»1/2″][vc_column_text css=»»]Es mundialmente conocido que el aumento en el abuso de fármacos es una tendencia que entraña peligros como las adicciones, las interacciones potencialmente mortales entre ellos o la aparición de resistencias entre las bacterias a las que deben combatir. Además, en los últimos años, las instituciones sanitarias cada vez revisan más la seguridad de los fármacos y la evaluación de los medicamentos de uso humano que se comercializan en nuestro país. Así, en los últimos años son numerosos los medicamentos que se han retirado o se les ha relacionado algún efecto adverso hasta ese momento desconocido. Y, normalmente, estas alertas o advertencias están asociadas a fármacos muy populares y usados en nuestro país.
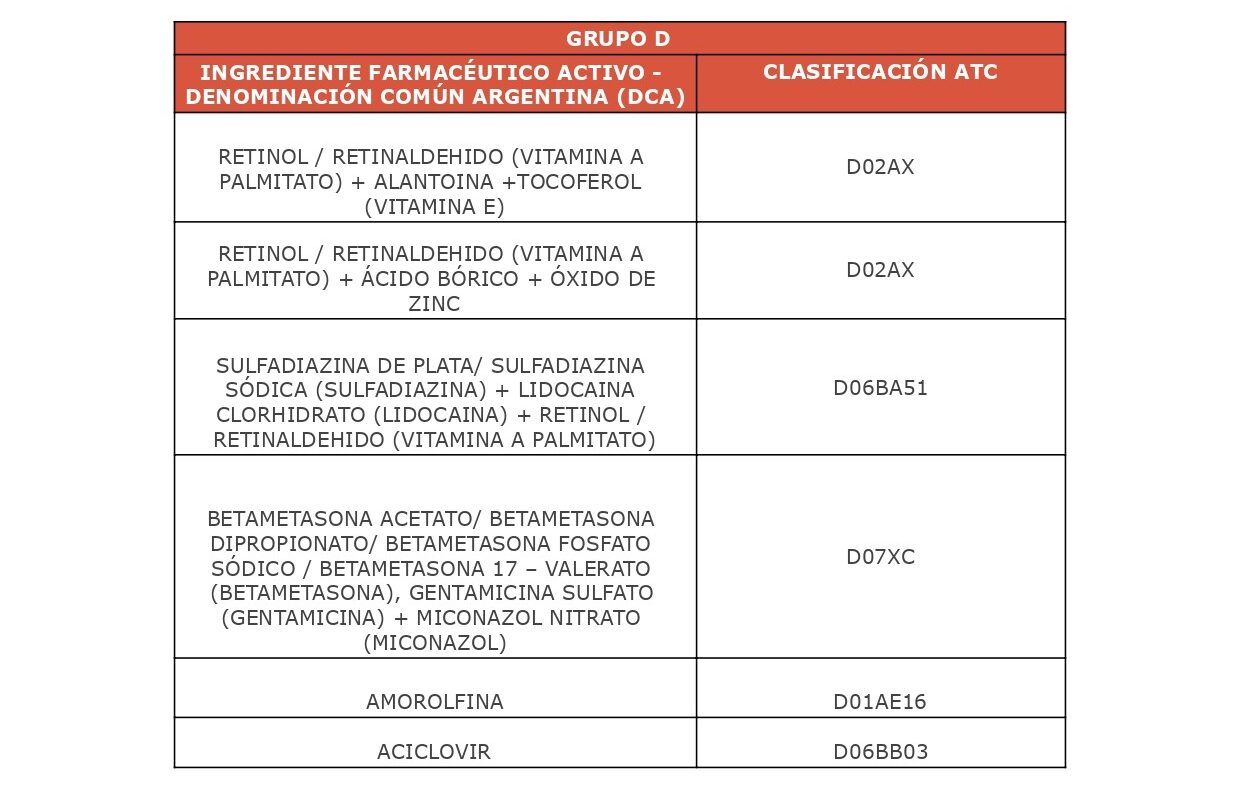
VITAMINA A + ALANTOINA + VITAMINA E:
Esta combinación en general se usa en forma tópica para pieles sensibles.
Como efectos adversos pueden presentarse enrojecimiento, hinchazón y picazón en la zona de aplicación.
Vitamina A: Debido a sus propiedades beneficiosas como agentes antioxidantes y a su papel para revertir el daño solar de la piel, se han añadido derivados de la vitamina A a los cosméticos. Aunque se utiliza ampliamente en cosméticos y fármacos tópicos, la dermatitis alérgica de contacto a la vitamina A y sus derivados no es poco común.
Vitamina E: la forma sintética de la vitamina E, el DL-tocoferol, que se ha utilizado ampliamente en ungüentos tópicos, puede causar dermatitis alérgica de contacto. Hay informes de dermatitis alérgica de contacto con erupción similar a eritema multiforme causada por un ungüento tópico. La prueba del parche indicó una reacción alérgica positiva a un ungüento antiinflamatorio que el paciente había estado usando y a su ingrediente, acetato de tocoferol.
El primer caso de Dermatitis Alérgica por Contacto (DAC) a vitamina E fue reportado en 1965 por Brodkin et al. en un paciente con dermatitis en el lóbulo de la oreja después de la aplicación local de una crema que contenía vitamina E. Desde entonces, se han descrito varios casos de DAC a vitamina E., contenida en desodorantes, aceites corporales, lociones para el cabello, y humectantes. La vitamina E fue el tercer alérgeno de contacto más común presente en 151 de 276 muestras de humectantes (55%), después de las fragancias (68 %) y parabenos (62%). El d,l-alfa-tocoferol (origen sintético) induce dermatitis con mayor frecuencia que el d-alfa-tocoferol (origen natural). Además, cuanto mayor sea la concentración de vitamina E en sus aceites puros, mayor será el riesgo de que causen DAC.
[mks_toggle title=»BIBLIOGRAFÍA» state=»close»]
Clemmensen, A., Thormann, J., & Andersen, K. E. (2007). Allergic contact dermatitis from retinyl palmitate in polycaprolactone. Contact Dermatitis (01051873), 56(5). https://pubmed.ncbi.nlm.nih.gov/17441856/
Bazzano C, de Angeles S, Kleist G, Macedo N. Allergic contact dermatitis from topical vitamins A and E. Contact Dermatitis. 1996;35(4):261‐262. https://pubmed.ncbi.nlm.nih.gov/8957661/
Kentaro Ohko, Akiko Ito, Masaaki Ito Allergic Contact Dermatitis Syndrome Due to Tocopherol Acetate, in Addition to Glycyrrhetinic Acid DLalfa-tocoferilo (vitamina E). Journal of Cosmetics, Dermatological Sciences and Applications Vol.2 No.1(2012) https://www.researchgate.net/publication/261064600_Allergic_Contact_Dermatitis_Syndrome_Due_to_Tocopherol_Acetate_in_Addition_to_Glycyrrhetinic_Acid
H. Saperstein, M. Rapaport and R. L. Rietschel, “Topical Vitamin E as a Cause of Erythema Multiforme-Like Eruption,” Archives of Dermatology, Vol. 120, No. 7, 1984, pp. 906-908. https://pubmed.ncbi.nlm.nih.gov/6233943/
R. H. Brodkin and J. Bleiberg, “Sensitivity to Topically Applied Vitamin E,” Archives of Dermatology, Vol. 92, No. 1, 1965, pp. 76-77. https://pubmed.ncbi.nlm.nih.gov/11850961/
J. Roed-Petersen and N. Hjorth, “Patch Test Sensitization from DL-alpha-tocopherol (Vitamin E),” Contact Dermatitis, Vol. 1, No. 6, 1975, p. 391. https://www.scirp.org/reference/referencespapers?referenceid=417753
A. C. de Groot, P. J. Berretty, C. J. van Ginkel, C. W. den Hengst, J. van Ulsen and J. W. Weyland, “Allergic Contact Dermatitis from Tocopheryl Acetate in Cosmetic Creams,” Contact Dermatitis, Vol. 25, No. 5, 1991, pp. 302-304. https://pubmed.ncbi.nlm.nih.gov/1809532/
B. Garcia-Bravo and P. Mozo, “Generalized Contact Dermatitis from Vitamin E,” Contact Dermatitis, Vol. 26, No. 4, 1992, p. 280. https://pubmed.ncbi.nlm.nih.gov/1395583/
T. Matsumura, T. Nakada and M. Iijima, “Widespread Contact Dermatitis from Tocopherol Acetate,” Contact Dermatitis, Vol. 51, No. 4, 2004, pp. 211-212. https://pubmed.ncbi.nlm.nih.gov/15500672/
A. Ramirez Santos, V. Fernandez-Redondo, L. Perez Perez, J. Concheiro Cao and J. Toribio, “Contact Allergy from Vitamins in Cosmetic Products,” Dermatitis, Vol. 19, No. 3, 2008, pp. 154-156. https://pubmed.ncbi.nlm.nih.gov/18627689/
Aeling JL, Panagotacos PJ, Andreozzi RJ. Allergic contact dermatitis to vitamin E aerosol deodorant. Arch Dermatol. 1973;108(4):579‐580 https://pubmed.ncbi.nlm.nih.gov/4745298/
Minkin W, Cohen HJ, Frank SB. Contact dermatitis from deodorants. Arch Dermatol. 1973;107(5):774‐775. https://pubmed.ncbi.nlm.nih.gov/4702716/
Goldman MP, Rapaport M. Contact dermatitis to vitamin E oil. J Am Acad Dermatol. 1986;14(1):133‐134. https://pubmed.ncbi.nlm.nih.gov/2936768/
Manzano D, Aguirre A, Gardeazabal J, Eizaguirre X, Pérez JLD. Allergic contact dermatitis from tocopheryl acetate (vitamin E) and retinol palmitate (vitamin A) in a moisturizing cream. Contact Dermatitis. 1994;31(5):324. https://pubmed.ncbi.nlm.nih.gov/7867333/
Zirwas MJ, Stechschulte SA. Moisturizer allergy. Diagnosis and management. J Clin Aesthet Dermatol. 2008;1(4):38‐44. https://pubmed.ncbi.nlm.nih.gov/21212847/
Kosari P, Alikhan A, Sockolov M, Feldman SR. Vitamin E and allergic contact dermatitis. Dermatitis. 2010;21(3):148‐153. https://pubmed.ncbi.nlm.nih.gov/20487657/
Fuente: Prospectos de especialidades medicinales.[/mks_toggle]
VITAMINA A + ACIDO BORICO + OXIDO DE ZINC:
Esta combinación en general se usa en forma tópica para el tratamiento de las dermatitis en bebes.
En general dicha combinación puede producir eczema o bien reacciones de hipersensibilidad.
ACIDO BORICO: Existen informes que demuestran la absorción del ácido bórico a través de la piel de los bebes. Se han informado tres casos de absorción transcutánea de ácido bórico en bebés tratados por dermatitis del pañal. Un niño murió. Esto generalmente ocurre cuando se aplica sobre piel dañada. Incluso las publicaciones sostienen de eliminar el ácido bórico de formulaciones tópicas para bebes y reemplazarlas por sustancias más seguras.
Se señala la especial sensibilidad de los lactantes a los efectos tóxicos del ácido bórico y se subraya la importancia de reconocer los casos más leves de intoxicación en este grupo de edad. Los hallazgos clínicos comunes consisten en erupciones cutáneas eritematosas seguidas de descamación, diarrea y vómitos, y evidencia de irritación meníngea. La presencia de ácido bórico en la orina y el líquido cefalorraquídeo se confirma fácilmente mediante la prueba del papel de cúrcuma.
Goldbloom y Goldbloom informaron de cuatro casos de intoxicación por ácido bórico en bebés, con síntomas de erupciones cutáneas eritematosas, diarrea y vómitos. Además, un quinto caso, un bebé de 27 días, presentó vómitos, convulsiones, eritema y descamación de la cara y el abdomen (Goldbloom y Goldbloom, 1953). Un bebé varón de 27 días de edad que había sido tratado por dermatitis con talco borado seguido de ácido bórico en polvo durante 7 días fue hospitalizado con gastroenteritis después de haber vomitado todas las tomas durante 3 días.
[mks_toggle title=»BIBLIOGRAFÍA» state=»close»]
M.D. James Ducey, M.D. D. Brooke Williams Transcutaneous absorption of boric acid The Journal of Pediatrics Volume 43, Issue 6, December 1953, Pages 644-651
https://pubmed.ncbi.nlm.nih.gov/13109661/
A.J. George Toxicity of boric acid through skin and mucous membranes Food and Cosmetics Toxicology Volume 3, 1965, Pages 99-101 https://pubmed.ncbi.nlm.nih.gov/14342801/
M.D. Richard B. Goldbloom Boric acid poisoning: Report of four cases and a review of 109 cases from the world literatura The Journal of Pediatrics Volume 43, Issue 6, December 1953, Pages 631-643 https://pubmed.ncbi.nlm.nih.gov/13109660/
Niels Hadrup Toxicity of boric acid, borax and other boron containing compounds: A review
Regulatory Toxicology and Pharmacology Volume 121, April 2021, 104873 https://pubmed.ncbi.nlm.nih.gov/33485927/
Antonio Lopalco, et al. Boric Acid, a Lewis Acid With Unique and Unusual Properties: Formulation Implications Journal of Pharmaceutical Sciences Volume 109, Issue 8, August 2020, Pages 2375-2386 https://pubmed.ncbi.nlm.nih.gov/32353453/
Fuente: Prospectos de especialidades medicinales[/mks_toggle]
SULFADIAZINA DE PLATA + LIDOCAINA + VITAMINA A:
LIDOCAINA: La lidocaína es un anestésico local tipo amida, sintetizado por primera vez entre 1943 y 1946 por Nils Löfgren y Bengt Lundquist, cuya función es bloquear los canales de sodio dependientes de voltaje (CSDV) en la porción interna de la membrana celular neuronal, interrumpiendo la transmisión nerviosa.
En pediatría, debe tenerse en cuenta que la aplicación de dosis altas o repetidas puede producir toxicidad sistémica. Esta se debe a la inhibición reversible de la generación y transmisión del impulso nervioso, teniendo efecto tanto estimulante como depresor a nivel del sistema nervioso central, y depresor sobre el cardiovascular. Entre las manifestaciones neurológicas destacan la confusión, alucinaciones, convulsiones, coma con apnea y, entre las cardiovasculares, la hipertensión y taquicardia transitorias seguidas de arritmias (bradicardia sinusal, arritmias del nodo AV y ventriculares, asistolia). Pueden aparecer náuseas y vómitos, así como metahemoglobinemia. Esta última, aunque posible, se relaciona más con intoxicaciones con otros anestésicos locales o combinaciones de estos, como la crema de lidocaína y prilocaína. Se han descrito casos pediátricos de intoxicación grave con dosis de lidocaína tópica entre 8,6-17,2mg/kg
La prevalencia de la dermatitis alérgica de contacto a la lidocaína está aumentando. Esto se debe a un número creciente de productos de venta libre que contienen anestésicos tópicos de amida y éster. Por otro lado, la lidocaína tópica puede ser segura en piel intacta pero en heridas contaminadas, puede provocar una respuesta inflamatoria exagerada.
[mks_toggle title=»BIBLIOGRAFÍA» state=»close»]
Piotr Zenon Szalaty Zachoszcz Toxicidad sistémica grave tras la aplicación de lidocaína tópica An Pediatr. 2023 Jun;98(6):472-474. https://pubmed.ncbi.nlm.nih.gov/37258317/
Martín-Zarco, J. G., García, P. O., & De Córdoba, J. L. F. (2003). Toxicidad por administración tópica de lidocaína. Acta Otorrinolaringológica Española, 54(9), 657-660. https://pubmed.ncbi.nlm.nih.gov/14992120/
To, D., Kossintseva, I., & de Gannes, G. (2014). Lidocaine contact allergy is becoming more prevalent. Dermatologic Surgery, 40(12), 1367-1372. https://pubmed.ncbi.nlm.nih.gov/25380091/
Duggan, M., Burns, D., Henry, M., & Mitchell, T. (1993). Reaction to topical lignocaine in a patient with contact dermatitis. Contact Dermatitis (01051873), 28(3). https://pubmed.ncbi.nlm.nih.gov/8462303/
[/mks_toggle]
SULFADIAZINA DE PLATA La sulfadiazina de plata (SDP) pertenece al grupo de las sulfas y se usa terapéuticamente en humanos mediante administración por vía tópica.
La sulfadiazina de plata inhibe la síntesis de ácido fólico y sus coenzimas, requeridas para la síntesis de precursores de ARN y ADN (purina y pirimidinas), y destruye a la bacteria por interferencia con la pared celular. Se formula principalmente como crema hidrosoluble blanca para ser usada como antiséptico en el tratamiento inmediato de emergencia en quemaduras térmicas y químicas, y en el desbridamiento de quemaduras. Es bactericida para un amplio rango de bacterias grampositivas y la mayoría de gramnegativas, incluidas las Pseudomonas aeruginosa y S. aureus
Debido a que no se ha demostrado eficacia de la sulfadiazina de plata y sí se conocen sus efectos adversos serios, la Agencia Francesa de Productos de Salud (ANSM, siglas en francés) ha recomendado restringir sus indicaciones a quemaduras de segundo grado o más graves. Sin embargo, incluso en estas situaciones, la prueba de su utilidad es deficiente.
En Francia, el agente antibacteriano sulfadiazina de plata se ha comercializado en forma de crema desde 1970 para su uso como antiséptico para heridas infectadas, quemaduras y «afecciones de la piel debido a infección bacteriana primaria o aquellas con susceptibilidad a infección secundaria».
La sulfadiazina de plata conlleva un riesgo de efectos adversos sistémicos serios comunes a las sulfonamidas, particularmente cuando se aplica sobre la piel dañada, una gran área superficial, o debajo de un vendaje oclusivo; estos incluyen trastornos hematológicos, renales y cutáneos. También se han informado, alteración de la conciencia y neuropatía periférica, relacionados con la absorción de plata a través de la piel.
A fines del año 2017, el Comité de la ANSM, responsable de la reevaluación de drogas, propuso la modificación del resumen de las características del producto (SPC) y el folleto de información, agregando una contraindicación de uso en niños menores de 2 años de edad, así como la mención de los siguientes efectos adversos serios: reacciones bullosas similares a síndrome de Stevens-Johnson y necrólisis epidérmica tóxica, citopenia (leucopenia, neutropenia y agranulocitosis) e insuficiencia renal.
Fuente: Silver sulfadiazine cream: disproportionate adverse effects. Prescrire International. September 2018. Volume 27 N° 196. Page 212. Disponible en: http://english.prescrire.org/en/SummaryDetail.aspx?Issueid=196
CONTRAINDICACIONES
La sulfadiazina de plata no deberá emplearse en los siguientes casos:
Discrasias sanguíneas.
Deficiencia en la glucosa-6-fosfato deshidrogenosa.
Deterioro de la función hepática.
Porfiria.
Deterioro de la función renal.
No emplear en pacientes sensibles a la sulfadiazina de plata, a otras sulfonamidas, furosemida, diuréticos de tiazida, sulfonilureas o inhibidores de la anhidrasa carbónica.
PRECAUCIONES
Las sulfonamidas pueden causar anemia hemolítica en los niños deficientes en la glucosa- 6-fosfato-dehidrogenasa (G6PD).
Pediatría: Su uso no se recomienda en prematuros o niños recién nacidos de hasta 1 mes de nacidos ya que las sulfonamidas pueden causar kernicterus en estos neonatos.
Geriatría: Debe valorarse la relación riesgo/beneficio.
EFECTOS INDESEABLES:
La sulfadiazina de plata puede ser absorbida después de una aplicación local y producir efectos sistémicos similares a otras sulfonamidas.
Las discracias sanguíneas (leucopenias transitorias) raramente requiere tratamiento, pero se recomienda monitoreo de las células sanguíneas para asegurarse que estas vuelvan a sus niveles normales pasados 5 días.
Puede ocurrir absorción sistémica de plata produciendo Argiria cuando el producto es aplicado en grandes áreas y por períodos prolongados. La Argiria se caracteriza por decoloración de la piel y neuropatía con trastornos sensitivos y motores.
Si la absorción que ocurre es significativa se pueden presentar los siguientes efectos adversos: Síndrome de Stevens-Johnson, Síndrome de Lyell’s, discrasias sanguíneas, cristalería.
Puede provocar reacciones alérgicas con deterioro de la función hepática y renal.
Se han reportado casos de reacciones, caracterizadas por ardor intenso que tiende a desaparecer, rash y prurito. En pacientes con amplia superficie quemada se produce absorción localmente de la sulfa con niveles en sangre que pueden llegar de 8 a 12 mg/ 100 mL, en estos casos puede producirse cristalería y debe hacerse control de las concentraciones de sulfa en sangre, hidratación del paciente con alcalinización de la orina para facilitar la disolución de los cristales evitando la cristalería. La superinfección por hongos de la superficie quemada, puede producirse, aunque no es frecuente la diseminación. En pacientes hipersensibles, pueden producirse reacciones similares a las producidas por los sulfoderivados
EMBARAZO Y LACTANCIA
Embarazo: Categoría de riesgo: B. Tercer trimestre: categoría de riesgo: D, por el riesgo de hemólisis. La absorción de las sulfonamidas puede desplazar la bilirrubina de los sitios de unión con la proteína en el plasma fetal, incrementando la posibilidad de kernicterus en el neonato.
Lactancia: Se desconoce que la sulfadiazina de plata, aplicada tópicamente se excrete en la leche materna. Sin embargo, la sulfadiazina de plata puede absorberse sistemáticamente en cantidades variables después de una aplicación local. Las mujeres en período de lactancia deben tener precaución puesto que las sulfonamidas administradas sistemáticamente son excretadas en la leche materna y puede causar kernicterus en lactantes o anemia hemolítica.
En Estados Unidos de Norteamérica Sulfadiazina de Plata al 1% crema (Silvadene®) es de venta bajo receta.
[mks_toggle title=»BIBLIOGRAFÍA» state=»close «]
Fuente:
https://medlineplus.gov/spanish/druginfo/meds/a682598-es.html
Astuto, Mariana et al Argiria generalizada secundaria a sulfadiazina de plata tópica Dermatol. argent ; 20(5): 335-338, 2014. ilus https://www.dermatolarg.org.ar/index.php/dermatolarg/article/view/1293/760
Fariña M., Escalonilla P., Grillic R., Soriano M. et ál. Argiria generalizada secundaria a la administración tópica de nitrato de plata, Actas Dermosifiliogr., 1998, 89: 547-552. https://actasdermo.org/es-argiria-generalizada-secundaria-administracion-topica-articulo-13003375
Flohr C, Heague J, Leach I, English J.Topical silver sulfadiazine-induced systemic argyria in a patient with severe generalized dystrophic epidermolysis bullosa. British Journal of Dermatology 159: 740-741, No. 3, 2008 – England https://pubmed.ncbi.nlm.nih.gov/18565180/
Browning J.C., Levi M.L. Argyria attributed to silvadene application in a patient with dystrophic epidermolysis bullosa, Dermatol. on line J., 2008, 14: 9 (2008) https://pubmed.ncbi.nlm.nih.gov/18627731/
Verena Isak, et al A Rare Case of Localized Argyria on the Face Case Reports in Dermatology 11(1):23-27 (2019) https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6477469/
Fisher NM, Marsh E, Lazova R. Scar-localized argyria secondary to silver sulfadiazene cream. J Am Acad Dermatol 2003;49(4):730-2 https://pubmed.ncbi.nlm.nih.gov/14512929/
Caffee F, Bingham H. Leukopenia and silver sulfadiazine. J Trauma. 1982;22: 586–587. https://pubmed.ncbi.nlm.nih.gov/7097818/
Jarret F, Ellerbe S, Demling R. Acute leukopenia during topical burn therapy with silver sulfadiazine. Amer J Surg. 1978; 135:818–819. https://pubmed.ncbi.nlm.nih.gov/665909/
Kiker RG, Carvajal HF, Micak RP, Larson DL. A controlled study of the effects of silver sulfadiazine on white blood cell counts in burned children. J Trauma. 1977; 17:835–836. https://pubmed.ncbi.nlm.nih.gov/335078/[/mks_toggle]
BETAMETASONA (ACETATO/DIPROPIONATO/FOSFATO SODICO/VALERATO) + GENTAMICINA SULFATO + MICONAZOL NITRATO:
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris – México) advierte a la población sobre el uso indiscriminado del medicamento con la combinación de betametasona, gentamicina y clotrimazol de uso tópico en presentación crema. El uso indiscriminado de este medicamento representa un grave riesgo a la salud de las y los pacientes, principalmente en población pediátrica, ya que se ha reportado que el uso excesivo y prolongado de la combinación de betametasona, gentamicina y clotrimazol por vía tópica (dérmica) puede causar diferentes reacciones adversas, entre las más graves, el Síndrome de Cushing.
Al respecto, es importante señalar que:
· El medicamento contiene un corticosteroide potente (betametasona), un antibiótico (gentamicina) y un antimicótico (clotrimazol); el cual está indicado para el tratamiento de diversas dermatosis.
· Debe tomarse en cuenta que, la aplicación incorrecta de este medicamento puede ocasionar efectos adversos locales y sistémicos, especialmente en pacientes pediátricos, entre ellos el síndrome de Cushing iatrogénico, un trastorno hormonal causado por la exposición prolongada del producto. Uno de los signos más frecuentes de este síndrome es la cara de “luna llena”, debido a que la grasa se deposita generalmente en la cara y alrededor del cuello; mientras que los brazos y las piernas se adelgazan. Los niños tienden a ser obesos con tasas de crecimiento más lento.
· Otros síntomas aparecen en la piel son fragilidad y delgadez. Los huesos se debilitan, hay un aumento en la presión arterial y se incrementan los niveles de glucosa (azúcar) en la sangre (hiperglucemia).
· Este medicamento es comúnmente utilizado en la población pediátrica mexicana por su fácil accesibilidad, por su bajo costo y por la falta de conocimiento de los efectos adversos que pueden sobrevenir con la aplicación de corticosteroides tópicos y sistémicos, en especial si se utilizan en áreas de piel delgada, lastimada y bajo oclusión, como la del pañal. Por lo que, si desarrollan síntomas, se deberá acudir con un profesional de la salud para atención médica.
[mks_toggle title=»FUENTE» state=»close «]Fuente: https://www.gob.mx/cms/uploads/attachment/file/859655/Aviso_de_Riesgo_uso_indiscriminado_de_BGC_04072023.pdf[/mks_toggle]
BETAMETASONA
Es un glucocorticoide sintético de acción prolongada con propiedades antiinflamatorias e inmunosupresoras que carece de propiedades mineralocorticoides prolongadas.
Si bien la administración tópica reduce la posibilidad de aparición de los efectos adversos sistémicos, no está exenta de ellos. En 1955, Malkinson y Ferguson, demostraron su absorción percutánea y, en 1962, Scoggins confirmó el descenso de cortisol en la orina debido a la administración por vía tópica de los corticoides.
Esto se debe a que el tratamiento con esteroides suprime la producción de hormona liberadora de corticotrofina y de ACTH, disminuye la síntesis adrenal de cortisol y origina la atrofia de las glándulas suprarrenales.
Dentro de los efectos adversos locales descritos por el mal uso y/o el uso prolongado de corticoides tópicos, se describen hipertricosis, dermatitis de contacto, telangiectasias, hipopigmentación, atrofia cutánea, dermatitis perioral, alteración de la cicatrización, púrpura, acné, estrías e infecciones locales oportunistas.
Entre los efectos adversos sistémicos descritos, además de la insuficiencia adrenal, se puede encontrar la presencia de cataratas, hipertensión arterial, hiperglucemia, glaucoma y osteonecrosis de la cabeza del fémur, entre otros
Aparte del efecto adverso intrínseco que presentan los corticoides tópicos, existen diversos factores externos que pueden modificar su absorción y que se deben tener en cuenta al momento de su utilización. Entre ellos, se puede mencionar la potencia del corticoide, el tipo de preparación, las cantidades utilizadas, la frecuencia de aplicación, la superficie por tratar, las zonas de oclusión, las características de la barrera cutánea y la edad del paciente
Finalmente, se debe remarcar que los niños, debido a la inmadurez de la barrera cutánea, son una población más predispuesta a los efectos adversos de los tratamientos tópicos.
Asimismo, está descripto para los corticoides tópicos la dermatitis alérgica:
Los pacientes con dermatitis alérgica de contacto por corticoides suelen presentar lesiones eccematosas subagudas o crónicas de larga evolución, aunque en raras ocasiones pueden aparecer eccemas agudos exudativos. Algunos de estos pacientes refieren empeoramiento de su dermatitis con la administración de corticoides tópicos, aunque la mayoría presenta unas lesiones que, aunque no son exacerbadas por éstos, tampoco responden de manera adecuada a ellos. La causa de este eccema inespecífico, que ocasiona su infradiagnóstico, se encuentra en las propiedades antiinflamatorias y alergénicas simultáneas que poseen los corticoides, enmascarando la sensibilización. Existe una serie de factores de riesgo para esta patología que actuarían como indicadores de pacientes vulnerables, como son las úlceras en miembros inferiores, la dermatitis de éstasis, las dermatitis crónicas, la sensibilización a múltiples medicamentos, la dermatitis de las manos y la dermatitis atópica.
Por todo ello es importante que los corticoides sean prescriptos sólo por médicos, es decir, que sea una medicación sujeta a control
La Betametasona es un corticoide tópico potente por lo que en Estados Unidos de Norteamérica es de venta bajo receta.
[mks_toggle title=»BIBLIOGRAFÍA» state=»close «]
Fuente: https://www.gob.mx/cms/uploads/attachment/file/859655/Aviso_de_Riesgo_uso_indiscriminado_de_BGC_04072023.pdf
Hengge UR, Ruzicka T, Schwartz RA, Cork MJ. Adverse effects of topical glucocorticosteroids. J Am Acad Dermatol. 2006;54(1):1-15. https://pubmed.ncbi.nlm.nih.gov/16384751/
Cheirif WO, Sáez de Ocariz MM, Lammoglia OL. Esteroides tópicos: revisión actualizada de sus indicaciones y efectos adversos en dermatología. Dermatología CMQ. 2015;13(4):305-12. https://www.medigraphic.com/pdfs/cosmetica/dcm-2015/dcm154e.pdf
EDELMAN, Solange; BUJAN, María M y CERVINI, Andrea B. Síndrome de Cushing iatrogénico secundario al mal uso de corticoïdes tópicos: Reporte de un caso pediátrico. Arch. argent. pediatr. [online]. 2019, vol.117, n.5 pp.e536-e539. http://www.scielo.org.ar/scielo.php?
Bockle BC, Jara D, Nindl W, Aberer W, et al. Adrenal insufficiency as a result of long-term misuse of topical corticosteroids. Dermatology. 2014; 228(4):289-93. https://pubmed.ncbi.nlm.nih.gov/24751677/
Cheirif WO, Sáez OMM, Lammoglia OL. Topical corticoids: current data, its indications and adverse effects in dermatology. Dermat CosmetMed Quir. 2015; 13(4):305-12. https://www.medigraphic.com/cgi-bin/new/resumenI.cgi?IDARTICULO=63461
Márquez Pardo R, Pérez Pelayo M, Aragoneses Calvo A, Gallego Rodríguez S, et al. Topical corticosteroids and secondary adrenal insufficiency: a relationship in the shade. Endocrinol Nutr. 2013; 60(9): e19-20. https://www.elsevier.es/en-revista-endocrinologia-nutricion-412-articulo-topical-corticosteroids-secondary-adrenal-insufficiency-S2173509313001797
Abraham G. Exogenous Cushing’s syndrome induced by surreptitious topical glucocorticosteroid overdose in infants with diaper dermatitis. J Pediatr Endocrinol Metab.2007; 20(11):1169-71. https://www.saem.org.ar/departamentos/departamento-neuroendocrinologia/cushing-exogeno.pdf
Siklar Z, Bostanci I, Atli O, Dallar Y. An infantile Cushing syndrome due to misuse of topical steroid. Pediatr Dermatol. 2004; 21(5):561-3. https://pubmed.ncbi.nlm.nih.gov/15461763/
Semiz S, Balci YI, Ergin S, Candemir M, et al. Two cases of Cushing’s syndrome due to overuse of topical steroid in the diaper area. Pediatr Dermatol. 2008; 25(5):544-7. https://pubmed.ncbi.nlm.nih.gov/18950396/
Diéguez Felechosa M, Valdés Gallego N, García-Alcalde Fernández ML, Casal Álvarez F. Hypoglycemia as a manifestation of iatrogenic adrenal insufficiency due to topical steroids. Endocrinol Nutr. 2013; 60(9): e21-2. https://www.elsevier.es/en-revista-endocrinologia-nutricion-412-articulo-hypoglycemia-as-manifestation-iatrogenic-adrenal-S2173509313001888
Nieman LK. Consequences of systemic absorption of topical glucocorticoids. J Am Acad Dermatol. 2011;65(1):250-2. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3775713/
MARTINEZ MARTINEZ, María Luisa et al. Dermatitis Alérgica de Contacto por Corticoides. Rev Clin Med Fam [online]. 2009, vol.2, n.8 pp.438-441 https://www.redalyc.org/pdf/1696/169614511010.pdf
[/mks_toggle]
GENTAMICINA SULFATO
Gentamicina es un antibiótico de la familia de los aminoglucósidos de administración parenteral y tópica.
La mayoría de los casos de dermatitis alérgica de contacto debida a gentamicina reportados en la literatura son relacionado con su uso tópico. La piel dañada favorece esta reacción.
[mks_toggle title=»BIBLIOGRAFÍA» state=»close «]
Thomas E. Drake, informa de un caso de tinnitus desarrollado por una paciente que usaba una crema con gentamicina al 0.1%.
Drake, T. E. (1974). Reaction to gentamicin sulfate cream. Archives of Dermatology, 110(4), 638-638. https://jamanetwork.com/journals/jamadermatology/article-abstract/534512
Green CM, Holden CR, Gawkrodger DJ. Contact allergy to topical medicaments becomes more
common with advancing age: an age-stratified study. Contact Dermatitis. 2007; 56:229-231. https://pubmed.ncbi.nlm.nih.gov/17343625/
[/mks_toggle]
MICONAZOL NITRATO
El nitrato de miconazol pertenece al grupo farmacológico de los antifúngicos de tipo azólico derivados del imidazo, el cual le confiere características básicas y es muy utilizado en medicina por sus propiedades antimicóticas. En dependencia de la forma farmacéutica se puede utilizar tanto como fármaco base o como sal: nitrato de miconazol.
[mks_toggle title=»BIBLIOGRAFÍA» state=»close «]
Wadi, T. R y cols., han informado sobre 10 pacientes que mostraron intolerancia al uso tópico de este fármaco. La mayoría de las reacciones fueron de naturaleza irritante, pero en dos casos se observó dermatitis alérgica de contacto.
Wadi, T. R., Jones, H. E., & Artis, W. A. (1979). Irritant and allergic reactions to topically applied Micatin® cream. Contact Dermatitis, 5(3), 168-170. https://pubmed.ncbi.nlm.nih.gov/455964/
Degreef, H., & Verhoeve, L. (1975). Contact dermatitis to miconazole nitrate. Contact Dermatitis (01051873), 1(4). https://pubmed.ncbi.nlm.nih.gov/139246/
Foged, F. K., & Hammershoy, O. (1982). Contact dermatitis due to miconazole nitrate. Contact Dermatitis (01051873), 8(4). https://pubmed.ncbi.nlm.nih.gov/7105701/
[/mks_toggle]
AMOROLFINA
La amorolfina o (2S,6R)-S2,6-dimetilo-4-(2-metilo-3-(4-[2-metilobutano-2) fenilo)propilo]morfolina es un derivado morfolínico de aplicación tópica que inhibe la D14 reductasa y la D7-8 isomerasa por lo que inhibe la síntesis de ergosterol (componente de la pared celular del hongo), alterando así la permeabilidad de la membrana celular y con ello el crecimiento del hongo. Estructuralmente no está relacionada con otros fármacos antimicóticos. Fue comercializada en diferentes países como laca de y se prescribe con frecuencia como laca de uñas para el tratamiento de la onicomicosis. Pueden producirse alteraciones de las uñas (por ejemplo, decoloración, rotura y uñas).
Uno de los efectos adversos más conocidos de las lacas con amorolfina es la dermatitis por contacto.
[mks_toggle title=»BIBLIOGRAFÍA» state=»close «]
K. Kramer, E. Paul. Contact dermatitis from amorolfine-containing cream and nail lacquer.
Contact Dermatitis, 34 (1996), pp. 145 https://pubmed.ncbi.nlm.nih.gov/8681549/
K. Kaneko, N. Aoki, M. Hata, J. Yajima, S. Kawana, S. Hattori. Allergic contact dermatitis from amorolfine cream. Contact Dermatitis, 37 (1997), pp. 307 https://pubmed.ncbi.nlm.nih.gov/9455645/
A. Fidalgo, L. Lobo. Allergic contact dermatitis due to amorolfine nail lacquer.
Dermatitis, 15 (2004), pp. 54 https://pubmed.ncbi.nlm.nih.gov/15573651/
Pérez-Varela L, Goday-Buján J, Piñeyro-Molina F, Costa-Domínguez C. Allergic contact dermatitis due to amorolfine in nail lacquer. Actas Dermosifiliogr. 2010;101:281-283. https://www.actasdermo.org/es-pdf-S1578219010706351
[/mks_toggle]
ACICLOVIR: Es un análogo acíclico del nucleósido natural 2 desoxiguanosina con actividad antiviral limitada a virus herpes. Dentro de las reacciones adversas del Aciclovir tópico:
Muy raramente:
Reacciones de hipersensibilidad inmediata incluyendo angioedema y urticaria.
Trastornos de los tejidos cutáneo y subcutáneo
Poco frecuentes:
• Ardor o pinchazos transitorios luego de la aplicación de ZOVIRAX® crema.
• Leve resecamiento o descamación de la piel.
• Prurito.
Raramente:
• Eritema.
[mks_toggle title=»BIBLIOGRAFÍA» state=»close «]
Fuente: Prospectos de las especialidades medicinales
A pesar del uso generalizado del aciclovir tópico, se ha informado de dermatitis alérgica de contacto causada por este fármaco.
Anca Chiriac MD, et al Allergic Contact Dermatitis from Topical Acyclovir: Case Series. The Journal of Emergency Medicine Volume 52, Issue 2, February 2017, Pages e37-e39 https://pubmed.ncbi.nlm.nih.gov/27658557/
Goday J, Aguirre A, Ibarra NG, Eizaguirre X. Allergic contact dermatitis from acyclovir.
Contact Dermatitis. 1991 May;24(5):380-1. https://pubmed.ncbi.nlm.nih.gov/1832623/
Bourezane Y, Girardin P, Aubin F, Vigan M, Adessi B, Humbert P, Laurent R. Allergy. Allergic contact dermatitis to Zovirax cream. 1996 Oct;51(10):755-6. https://pubmed.ncbi.nlm.nih.gov/8905006/
Camarasa JG, Serra-Baldrich E. Allergic contact dermatitis from acyclovir.
Contact Dermatitis. 1988 Sep;19(3):235-6. https://pubmed.ncbi.nlm.nih.gov/3191693/
Vernassiere C, Barbaud A, Trechot PH, Weber-Muller F, Schmutz Systemic acyclovir reaction subsequent to acyclovir contact allergy: which systemic antiviral drug should then be used?
JL. Contact Dermatitis. 2003 Sep;49(3):155-7. https://pubmed.ncbi.nlm.nih.gov/14678212/.
Colombina Vincenzi, et al Allergic Contact Dermatitis Caused by Acyclovir American Journal of Contact DermatitisVol. 3, No. 2: 105-107 (1992) https://www.liebertpub.com/doi/abs/10.1053/ajcd.1992.2404?download=true&journalCode=ajcd
[/mks_toggle]
En Estados Unidos la crema de Aciclovir (Zovirax®) es de venta bajo receta.
Farm. ALEJANDRA MARIANA GÓMEZ
Presidente Colegio de Farmacéuticos de la Pcia. de Bs. As
Red Provincial de Vigilancia Farmacéutica
[/vc_column_text][/vc_column][vc_column width=»1/4″][/vc_column][/vc_row]